Электроотрицательность - ключевое понятие в химии, которое позволяет определить, насколько атом способен притягивать к себе электроны.
Определение электроотрицательности было введено Линусом Полингом в 1932 году и стало важным инструментом для понимания свойств элементов и их химического поведения.
Электроотрицательность атома зависит от электронной конфигурации, размера и заряда ядра. Чем больше эти параметры, тем сильнее атом притягивает электроны. В таблице Менделеева электроотрицательность элементов обозначается числовым значением от 0 до 4.
Что такое электроотрицательность?

Электроотрицательность обратно пропорциональна радиусу атома: чем меньше размер атома, тем больше его электроотрицательность. Она также зависит от положения элемента в периодической системе, увеличиваясь по группе снизу вверх и вдоль периода слева направо.
Электроотрицательность измеряется с использованием шкалы Полинга или шкалы Малликена–Хэмметта. Фтор считается самым электроотрицательным элементом с максимальным значением 4. Водород имеет значение 2.1 и является референсным элементом для сравнения с другими.
Знание электроотрицательности элементов помогает определить тип химической связи между ними. Если разница в электроотрицательности двух атомов, образующих связь, невелика или равна нулю, то связь считается неполярной (например, в молекуле кислорода O2). Если разница в электроотрицательности составляет от 0.4 до 1.9, то связь считается полярной (например, в молекуле воды H2O). Если разница в электроотрицательности больше 1.9, то связь считается ионной (например, в молекуле кухонной соли NaCl).
Определение и смысл понятия

Определение электроотрицательности в химии впервые было предложено Линусом Полингом в 1932 году. Он создал шкалу электроотрицательности, известную как шкала Полинга, где максимальное значение отводится флуору (4.0) и минимальное - цезию и францию (0.7).
С другой стороны, существуют эмпирические шкалы, основанные на измерении сил, включая энергию атомных связей, диссоциационную энергию и поляризуемость. Одна из наиболее известных таких шкал - шкала Полинга. Она выражается формулой:
χ = 0.208(EN) + 0.691(IE) + 0.279(EA) + 0.019(P]
где:
- χ - электроотрицательность элемента;
- EN - энергия связи элемента с водородом;
- IE - энергия ионизации элемента;
- EA - энергия аффинности элемента;
- P - поляризуемость элемента.
Обратите внимание, что эти формулы являются приближенными, их использование может давать только относительную электроотрицательность элементов.
Различные подходы и методы
В химии существует несколько способов определения электроотрицательности элементов.
- Метод Полинга. Этот метод базируется на измерении электроотрицательности элементов относительно водорода, который имеет сканирующую нулевую электроотрицательность.
- Шкала Полинга. Разработанная Линусом Полингом, шкала позволяет сравнивать электроотрицательности различных элементов. Шкала Полинга начинается от единицы и доходит до значения 4, самое высокое из которых принадлежит флуору.
- Метод Полинга-мю. Данный метод учитывает атомные массы элементов в качестве дополнительных факторов.
- Метод электротермической эквилибрации. Этот метод основан на измерении теплового равновесия между двумя различными веществами с разными электроотрицательностями.
Выбор метода определения электроотрицательности зависит от цели и особенностей исследования.
Значение электроотрицательности в химических связях

Значение электроотрицательности в химических связях играет решающую роль в определении их характера. Если разность электроотрицательности между атомами невелика или равна нулю, то связь будет неполярной, так как электроны будут равномерно распределены между атомами.
В случае, когда разность электроотрицательности между атомами больше нуля, возникает полярная химическая связь. В таких связях электроны смещаются ближе к атому с большей электроотрицательностью, что приводит к образованию положительного и отрицательного полюсов.
Электроотрицательность используется для предсказания химических свойств веществ. Например, вода с высокой электроотрицательностью образует водородные связи и имеет высокую температуру кипения. Молекулы с малой разностью электроотрицательности обычно имеют низкую температуру кипения и плавления.
Таким образом, электроотрицательность играет важную роль в химических связях и свойствах веществ.
Влияние на силу и тип связей
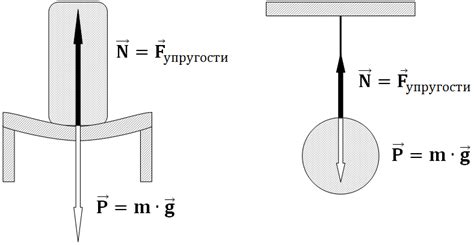
При разнице в электроотрицательности меньше 0,5 образуется неполярная ковалентная связь, где электроны равномерно распределены между атомами и не создают полярности.
Если разница в электроотрицательности между атомами от 0,5 до 1,9, то образуется полярная ковалентная связь, где электроны неодинаково распределены.
Если разница в электроотрицательности больше 1,9, то возникает ионная связь, где электроны полностью передаются от одного атома к другому.
Электроотрицательность определяет силу и тип химической связи, помогая понять химические связи в различных соединениях.
Электроотрицательность в периодической таблице
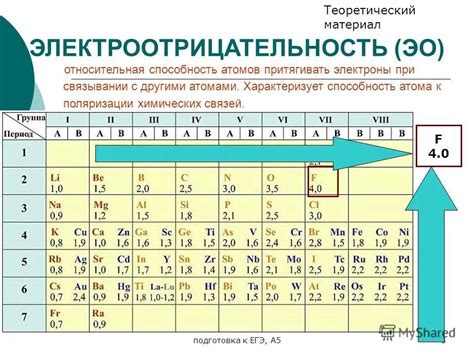
Элементы в периодической таблице упорядочены по атомным номерам. Электроотрицательность чаще всего увеличивается слева направо и уменьшается сверху вниз.
Флуор (F) и хлор (Cl) самые электроотрицательные элементы, находятся в правом верхнем углу таблицы. Они лучше всего притягивают электроны. Щелочные металлы, такие как литий (Li) и натрий (Na), самые электронноположительные элементы, расположены в левом нижнем углу.
Электроотрицательность элементов помогает понять химические свойства веществ. Она предсказывает типы химических связей и свойства соединений, а также влияет на реакционные пути. Знание электроотрицательности помогает анализировать и объяснять химические явления и реакции.
Важно учитывать, что электроотрицательность - лишь одна из характеристик элементов. Она используется совместно с другими свойствами для полного понимания химической природы вещества.
Тренды и закономерности

Один из основных трендов в электроотрицательности связан с периодической таблицей. Электроотрицательность увеличивается с увеличением порядковых номеров элементов и уменьшением атомных радиусов. Например, хлор (Cl) имеет более высокую электроотрицательность, чем калий (K), потому что хлор имеет меньший атомный радиус и находится правее в таблице.
Еще один тренд связан с группами элементов. Электроотрицательность увеличивается сверху вниз по группе. Например, кислород (O) имеет более высокую электроотрицательность, чем сера (S), потому что кислород находится выше серы в группе.
Электроотрицательность зависит от размера и заряда ядра. Например, у металлов, которые имеют больший размер и меньший заряд ядра, электроотрицательность обычно ниже.
Электроотрицательность - одна из химических характеристик элементов, которая не всегда полностью определяет их поведение. Структура молекулы и наличие функциональных групп также важны для понимания химической активности элементов.