Химические формулы - это комбинации символов, идентифицирующие вещества и соединения. Одним из распространенных типов формул являются формулы оснований.
Основание - класс веществ с низкой кислотностью, образующих гидроксиды. Они важны в химических реакциях и применяются широко.
Определение основания в химии по формуле может быть простым, если вы знаете некоторые основные принципы и правила. Основания обычно содержат гидроксидную группу (OH) в начале или середине формулы. Также могут содержаться металлы или их группы, такие как натрий (Na), калий (K) или магний (Mg).
Что такое основание
Основания делятся на гидроксиды металлов и неорганические основания. Гидроксиды металлов состоят из металла и группы OH-. Примеры: гидроксид натрия (NaOH), гидроксид калия (KOH) и гидроксид алюминия (Al(OH)3).
Неорганические основания не содержат металлов, вместо этого они состоят из анионов, таких как аммоний (NH4+) или гидроксидный ион (OH-). Примерами неорганических оснований являются аммиак (NH3), аммонийная селитра (NH4NO3) и аммонийная сода (NH4HCO3).
Основания играют важную роль в химических реакциях и находят широкое применение в промышленности, медицине и быту. Использование оснований позволяет выполнять множество процессов, таких как нейтрализация кислот, очистка воды и производство удобрений.
| Гидроксид металла | Неорганическое основание |
|---|---|
| NaOH (гидроксид натрия) | NH3 (аммиак) |
| KOH (гидроксид калия) | NH4NO3 (аммонийная селитра) |
| Al(OH)3 (гидроксид алюминия) | NH4HCO3 (аммонийная сода) |
Определение основания в химии
Основания можно определить по их химической формуле. Формула основания часто состоит из металла (или аммония), за которым следует гидроксидная группа OH с зарядом -1.
Для определения основания в химии можно использовать таблицу с именами и формулами основных веществ, а также их зарядом при взаимодействии с кислотой.
| Имя основания | Формула | Заряд |
|---|---|---|
| Гидроксид натрия | NaOH | -1 |
| Гидроксид калия | KOH | -1 |
| Гидроксид аммония | NH4OH | -1 |
При взаимодействии основания с кислотой происходит нейтрализационная реакция. В результате образуется соль и вода. Основания играют важную роль в химических и биологических процессах.
Используя знания о формуле и свойствах оснований, можно определить их в химических реакциях и применять в различных областях науки и технологии.
Как определить основание
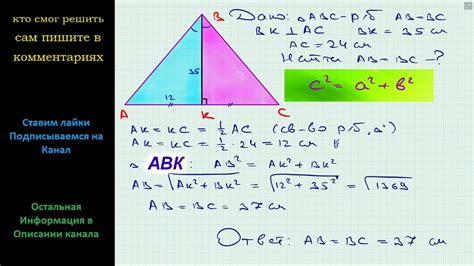
Для определения основания можно использовать формулу вещества. Обычно они имеют формулу MX(OH)n, где M - металл, X - анион, n - количество гидроксильных групп.
Основания можно также определить по их свойствам. Сильные основания полностью диссоциируют в растворе и образуют большое количество гидроксидионов, а слабые основания диссоциируют частично и образуют меньшее количество гидроксидионов.
Основания имеют щелочную реакцию, образуя гидроксиды при контакте с водой. Это помогает определить их - если вещество реагирует с водой, образуя гидроксид, то оно, скорее всего, основание.
Основания обладают такими свойствами, как щелочной вкус, способность нейтрализовать кислоты, образовывать с ними соли и формировать тугоплавкие оксиды.
Определение основания важно для понимания его свойств и роли в реакциях, а также для установления соотношения между кислотами и основаниями - важного понятия в химии.
Методы определения основания

Качественный анализ
Этот метод позволяет определить основание на основе его химических свойств и реакций.
Основание может быть ионным или молекулярным. Для определения ионных оснований используют реакции с кислотами и индикаторные растворы.
Молекулярные основания определяют по своим физическим свойствам, таким как растворимость, плавление и кипение.
Количественный анализ
Количественный анализ позволяет определить содержание основания в растворе. Для этого используют титрование, гравиметрию и спектрофотометрию.
Титрование основано на реакции основания с кислотой известной концентрации. Измеряя количество добавленной кислоты до нейтрализации, можно определить концентрацию основания.
Гравиметрический анализ основывается на определении массы осадка, полученного при реакции основания с раствором соответствующего соли. Спектрофотометрия позволяет измерять поглощение или прохождение света основанием и на основе полученных данных определить его концентрацию.
Основания в химических реакциях

Основания играют ключевую роль во многих химических процессах, таких как нейтрализация кислот, гидролиз, образование комплексных соединений и др. Они могут быть использованы в различных областях, включая промышленность, лабораторную практику и медицину.
Определение основания в химии осуществляется по формуле соединения. Обычно основания содержат гидроксильные группы (OH-) или аминогруппы. Гидроксиды металлов, такие как гидроксид натрия (NaOH) или гидроксид калия (KOH), являются примерами оснований, содержащих гидроксильные группы.
При взаимодействии основания с кислотой образуется соль и вода. Например, гидроксид натрия и хлороводородная кислота (HCl) образуют соль NaCl и воду (H2O).
Важно помнить, что не все соединения с гидроксильными или аминогруппами являются основаниями. Определение основания требует анализа структуры соединения и его свойств.
Роль основания в реакциях

Основания в реакциях могут образовывать соли и воду. Такие реакции обычно называют нейтрализационными, поскольку основания "нейтрализуют" кислоты, образуя соли.
Основания могут использоваться в различных реакциях. Например, в окислительно-восстановительных реакциях они могут действовать как восстановители или окислители.
Также основания играют важную роль в образовании комплексных соединений, образуя стабильные комплексы с металлами и другими веществами.
Понимание функций оснований в химических реакциях существенно для изучения свойств химических соединений и их применения, например, в синтезе органических соединений, производстве лекарств и анализе соединений.
Взаимодействие оснований с кислотами

Когда основание встречается с кислотой, происходит нейтрализация. Они теряют свою активность и образуют соль и воду. Например, NaOH (основание) + HCl (кислота) → NaCl (соль) + H2O (вода).
Основание (NaOH) и кислота (HCl) соединяются, образуя соль (NaCl) и воду (H2O).
Основание имеет особую структуру: металл (например, натрий или калий), атом кислорода и гидроксильная группа (OH-), позволяющая основанию участвовать в реакциях.
Кислота содержит протон (H+), основание отдает электроны таким образом, в результате образуется вода и соль.
Это важное взаимодействие основания с кислотой используется в различных областях, таких как фармацевтика, пищевая промышленность и производство удобрений, что помогает химикам улучшать продукцию.
Определение основания в реакции с кислотой
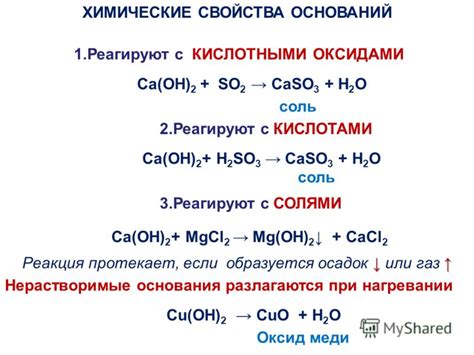
Определение основания в реакции с кислотой основано на реакции нейтрализации, при которой кислота и основание взаимодействуют, образуя соль и воду. Основание обычно представляет собой вещество, которое способно принять протон (H+) от кислоты.
Для определения основания в реакции с кислотой, необходимо рассмотреть уравнение реакции и обратить внимание на вещества, которые образуются. Основание обычно будет присутствовать в виде аниона в полученной соли.
| Примеры оснований | Соответствующая соль |
|---|---|
| Гидроксид натрия (NaOH) | Na+ + OH- → NaOH |
| Гидроксид калия (KOH) | K+ + OH- → KOH |
| Гидроксид аммония (NH4OH) | NH4+ + OH- → NH4OH |
Основание может быть представлено в виде аммония (NH4+) или металла, соединенного с гидроксидной группой (OH-).
Для определения основания в реакции с кислотой, необходимо изучить вещества, образующиеся в результате реакции нейтрализации и определить наличие аниона или аммония, соединенного с гидроксидной группой.
Основания в органической химии
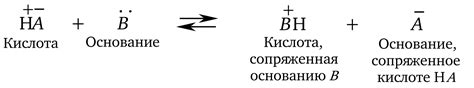
Основания могут быть неорганического или органического происхождения. Неорганические основания, такие как гидроксид натрия (NaOH) или гидроксид калия (KOH), чаще используются для нейтрализации кислот или регулирования pH-значения растворов.
Органические основания - это сложные соединения с атомами азота, аминогруппами (-NH2) или ароматическими циклами, как пиридиновые основания. Они широко используются в органическом синтезе для создания новых связей и структурных элементов.
Основания могут действовать как нуклеофилы, атакуя электрофильные центры в молекуле, или активировать ацетиленовые связи для их превращения в более устойчивые структуры.
Основания применяются не только в химическом синтезе, но и в фармацевтической и пищевой промышленности, а также в медицине для создания препаратов и лекарств.
Зная эти признаки, можно с большой вероятностью предположить, является ли данное органическое соединение основанием. Однако, для более точного определения основания может потребоваться проведение химического анализа с использованием специальных реактивов и методов.