Фонарики – незаменимые помощники в условиях недостатка освещения. Они сопровождают нас в походах, путешествиях и в экстренных ситуациях. Однако, необходимой составляющей их работы является работающая батарейка. Но как же работает батарейка в фонарике и как она обеспечивает постоянную подачу питания?
Батарейка работает благодаря электрохимической реакции между положительным и отрицательным электродами через электролит. Обычно в качестве электродов используют цинк или уголь, а в качестве электролита - раствор солей. Электрохимическая реакция запускается, когда батарейка замкнута в устройстве, таком как фонарик, и продолжает работать до тех пор, пока есть свободные электроны.
Свободные электроны двигаются внутри батарейки, создавая электрический ток. Отрицательные электроны переходят с отрицательного электрода на положительный через электролит, обеспечивая работу устройства. Но когда батарейка разряжается, электроны перестают двигаться, и ток прекращается.
Батарейка в фонарике работает по принципу химической реакции, которая происходит между разными веществами внутри батарейки. Эта реакция производит электричество, которое затем используется для питания лампочки в фонарике и создания света.
Принцип работы батарейки в фонарике

При включении фонарика схема внутри батарейки закрывается, и начинается электрический ток, за счет которого электроны начинают двигаться от анода к катоду, создавая электрический потенциал, который питает фонарик.
Анод состоит из цинка и расположен внутри батарейки. Катод состоит из марганца диоксида и окиси марганца и находится на верхней стороне батарейки. Между ними находится электролитическая среда, которая позволяет ионам перемещаться через батарейку и обеспечивает химическую реакцию.
При работе батарейки цинк с анода окисляется, отдавая электроны в катод. В то же время, оксид марганца в катоде принимает электроны, что инициирует химическую реакцию, обеспечивающую поток электронов.
Щелочные батарейки обеспечивают стабильный ток и имеют длительный срок службы. Когда реакции внутри батарейки заканчиваются, она перестает выдавать достаточное напряжение и нуждается в замене.
Батарейки позволяют фонарику работать даже без электричества, обеспечивая свет и безопасность в темноте.
Процесс химической реакции

Батарейки в фонариках производят электрическую энергию через химическую реакцию внутри себя. Внутри батарейки содержится два разных химических вещества, которые называются электродами. Один электрод положительно заряжен и называется катодом, а другой отрицательно заряжен и называется анодом. Между ними находится электролит, который позволяет проходить электронам.
Когда фонарик включается, один из электродов начинает терять электроны, которые перемещаются через электролит к другому электроду. Этот электрод получает электроны и заряжается. Таким образом, между катодом и анодом возникает разность потенциалов, или напряжение. Это напряжение позволяет электронам двигаться и создает электрический ток, который питает лампу.
В химической реакции в батарейке вещества в электродах меняются, что приводит к ее разрядке. Когда одно из веществ исчезает, батарейка перестает работать и требует замены.
Реакция в батарейке может быть обратимой или необратимой, в зависимости от типа. Перезаряжаемые батарейки могут быть восстановлены при подключении к источнику напряжения. Но не все батарейки перезаряжаемы, после разряда их нужно утилизировать.
Электрический потенциал

В батарейке создается электрический потенциал между положительным и отрицательным электродами, вызывая появление электрического поля.
При включении фонарика электрическое поле заставляет электроны двигаться от отрицательного к положительному электроду, передавая свою энергию другим электронам и создавая световой эффект.
Электрический потенциал позволяет передавать энергию и создавать свет как в батарейке, так и во всей системе, включая фонарик. При разряде батарейки потенциал уменьшается, что приводит к уменьшению яркости света.
Функции электродов

Анод – положительный электрод, который выделяет электроны. Когда батарейка вставляется в фонарик, анод отдает электроны на катод.
Катод – отрицательный электрод, который принимает электроны от анода. Перемещаясь на катод, электроны создают электрический ток внутри батарейки.
Электроды обеспечивают поток электронов, необходимый для работы батарейки, питающей фонарик.
Роль электролита
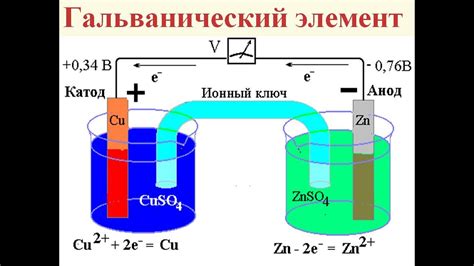
Электролит – вещество, проводящее электрический заряд. В батарейке фонарика применяется электролит на основе щелочи, такой как гидроксид калия или гидроксид натрия, находящийся между анодом и катодом.
При включенном фонарике происходит химическая реакция между анодом и катодом через электролит. Электроны начинают двигаться, создавая электрический ток, который питает лампочку и заставляет её светиться.
Электролит не участвует в процессе генерации электрической энергии. Он лишь проводит заряд между анодом и катодом. Время от времени электролит может повредиться или истощиться, что снизит производительность батарейки.
Из-за важной роли электролита нужно аккуратно обращаться с батарейкой фонарика. Повреждение или разлив электролита может вызвать коррозию и деградацию батарейки, поэтому важно следовать инструкциям производителя и не открывать батарейку самостоятельно.