Удельная теплота сгорания показывает количество энергии, выделяющееся при сгорании вещества. Этот параметр важен в физике, химии и энергетике.
Для расчета удельной теплоты сгорания используется формула:
Удельная теплота сгорания = количество энергии / масса сгоревшего вещества
Удельная теплота сгорания - это важный параметр для проектирования и оптимизации процессов сжигания различных веществ, таких как углеводороды, алкоголи, карбонаты и другие. Этот параметр также используется при использовании веществ в качестве топлива или энергоносителя.
Правильный расчет удельной теплоты сгорания является основой для оптимизации энергетических процессов и разработки эффективных технологий. Также он может служить для оценки экологической устойчивости вещества, так как высокая удельная теплота сгорания может указывать на большое количество выделяемых при сгорании вредных веществ.
Что такое удельная теплота сгорания и как ее получить
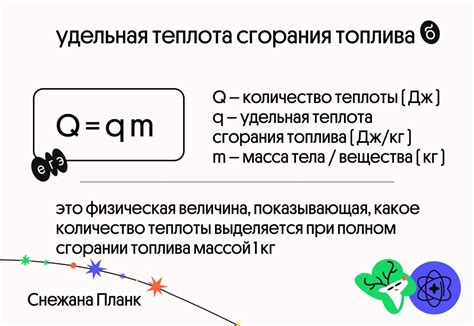
Удельную теплоту сгорания обычно измеряют в джоулях на грамм (Дж/г) или в калориях на грамм (кал/г). Для расчета удельной теплоты сгорания используется следующая формула:
| Удельная теплота сгорания (Q) | = | Выделившееся тепло (Qвыдел.) | / | Масса сгоревшего вещества (m) |
|---|
where:
Q - удельная теплота сгорания;
Qвыдел. - выделившееся тепло;
m - масса сгоревшего вещества.
Чтобы получить удельную теплоту сгорания, необходимо измерить выделившееся тепло вещества при его полном сгорании и затем разделить его на массу сгоревшего вещества.
Лабораторные методы исследования позволяют точно измерить выделившееся тепло, используя калориметр. Калориметр – это прибор, предназначенный для определения количества выделяющегося или поглощаемого тепла при химических реакциях.
Удельная теплота сгорания является важной характеристикой различных веществ. Ее знание позволяет определить тепловую эффективность сгорания и использовать энергию, выделяющуюся в результате сжигания веществ.
Физическое понятие удельной теплоты сгорания
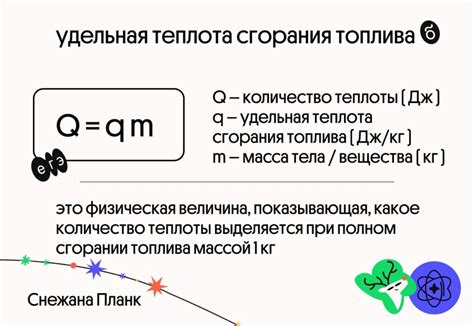
Удельная теплота сгорания измеряется в джоулях на грамм (Дж/г) или килоджоулях на грамм (кДж/г). Она позволяет оценить, насколько тепловой энергии можно получить при сгорании данного вещества.
Удельная теплота сгорания зависит от химического состава вещества и может быть различной для разных веществ.
Для расчета удельной теплоты сгорания обычно используется следующая формула:
- Найти количество теплоты, выделяющееся при сгорании данного вещества.
- Разделить это количество на массу сгоревшего вещества.
Полученное значение будет удельной теплотой сгорания.
Удельная теплота сгорания важна для оптимизации использования топлива и оценки его эффективности. Знание удельной теплоты сгорания позволяет проводить расчеты и прогнозировать количество выделяющегося тепла при сгорании различных веществ.
Практическое применение удельной теплоты сгорания
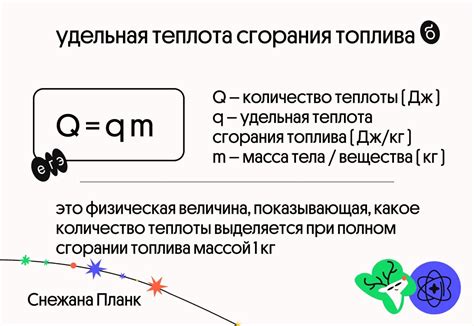
Удельная теплота сгорания используется для оценки энергетической эффективности топлива. Чем выше удельная теплота сгорания, тем больше энергии вы получите. Это помогает выбирать экономичные и эффективные источники энергии.
Теплота сгорания также важна при расчете систем отопления. Выбор топлива зависит от удельной теплоты сгорания. Чем выше удельная теплота сгорания, тем эффективнее будет система отопления.
Знание удельной теплоты сгорания помогает определить количество выделяющегося тепла при сгорании топлива и использовать его для различных целей.
Формула и методика расчета

Формула для удельной теплоты сгорания:
Qсыр = Qполн / m,
где Qсыр – удельная теплота сгорания (Дж/кг), Qполн – полная теплота сгорания (Дж), m – масса вещества (кг).
Шаги для расчета удельной теплоты сгорания:
- Определить массу сгоревшего вещества.
- Измерить полную теплоту сгорания вещества с помощью специального оборудования.
- Подставить значения в формулу и выполнить вычисления.
Результат расчета позволяет определить удельную теплоту сгорания вещества в единицах энергии на единицу массы. Полученная величина важна для понимания термических свойств материалов и для прогнозирования их применения в промышленности.
Пример расчета удельной теплоты сгорания

Для расчета удельной теплоты сгорания (Q) вещества нужно знать массу вещества (m) и количество выделенной теплоты (Qвыделенная). Удельная теплота сгорания (Qудельная) рассчитывается по формуле:
Qудельная = Qвыделенная / m
У нас есть 1 кг древесины, и при сгорании выделяется 16 МДж теплоты. Удельная теплота сгорания древесины: 16 МДж/кг.
| Масса (м) | Теплота (Qвыделенная) | Удельная теплота (Qудельная) |
|---|---|---|
| 1 кг | 16 МДж | 16 МДж/кг |
Это значит, что при сгорании 1 кг древесины выделяется 16 МДж теплоты.
Значимость удельной теплоты сгорания в современной науке и промышленности

В современной науке и промышленности удельная теплота сгорания играет важную роль, определяя энергетическую эффективность топлива и веществ в технологических процессах.
Удельная теплота сгорания позволяет проводить расчеты и сравнивать различные виды топлива по их энергетической эффективности. Это важно при выборе оптимального топлива для технических процессов.
Этот параметр также важен при разработке и исследовании новых материалов, веществ и топлив. Знание удельной теплоты сгорания помогает определить эффективность и безопасность использования новых материалов в промышленности.
Удельная теплота сгорания позволяет:
- Оценить энергетическую эффективность топлива;
- Сравнивать различные виды топлива;
- Предсказать количество выделяющегося тепла при сгорании;
- Разрабатывать новые материалы и вещества с оптимальными энергетическими характеристиками.
Удельная теплота сгорания играет важную роль в науке и промышленности, позволяя определить энергетическую эффективность различных веществ и топлива для выбора оптимальных решений и повышения энергетической эффективности технических и промышленных процессов.