Гибридизация - важное понятие в органической химии, определяющее пространственную структуру молекулы и влияние на химические свойства вещества. Гибридизация атомов в органических соединениях позволяет определить типы связей в молекуле и предсказать свойства и реакционную способность соединения.
Существует несколько методов определения типа гибридизации атомов. Один из них - это анализ геометрии молекулы. Если в молекуле атомы имеют линейную арендацию, то это говорит о сп2-гибридизации. Если атомы имеют плоско-треугольную геометрию, то это означает, что атомы гибридизированы по сп2-гибридизации. И, наконец, если атомы располагаются в треугольной пирамидальной структуре, то это свидетельствует о сп3-гибридизации.
Еще одним методом определения типа гибридизации является анализ энергии связи между атомами. Связь между атомами, образованная путем гибридизации, обычно является более крепкой и имеет более высокую энергию связи. Это можно установить путем измерения длины связи между атомами в молекуле. Если связь короткая и имеет большую энергию, то это может указывать на наличие гибридизации.
Определение гибридизации
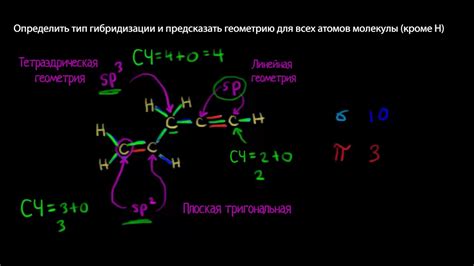
Гибридизация в органических соединениях определяется по геометрии молекулы и количеству связей атомов. Основные методы включают:
- Рассмотрение электронных групп вокруг атома: учитывается количество электронных групп, связанных с атомом. Например, атом с 4 группами имеет sp3-гибридизацию.
- Анализ геометрии молекулы: гибридизацию атома можно определить по геометрии молекулы. Например, при линейной форме молекулы атомы скорее всего имеют sp-гибридизацию.
- Использование связующих атомных орбиталей: для определения гибридизации в органических соединениях можно использовать связующие атомные орбитали. Например, если орбиталь атома перекрывается с связующими атомными орбиталями через связь с двумя электронными парами, то атом имеет sp2-гибридизацию.
Определение гибридизации важно в органической химии, так как тип гибридизации атома влияет на его химические свойства и способность образовывать связи с другими атомами.
Методы определения гибридизации
1. Спектроскопические методы:
Спектроскопия, такая как ИК-спектроскопия и ЯМР-спектроскопия, позволяют исследовать электронную структуру органических соединений. Гибридизация атомов влияет на частоту колебаний химических связей и химические сдвиги сигналов в спектрах, что позволяет определить тип гибридизации атомов.
2. Рентгеноструктурный анализ:
Метод рентгеноструктурного анализа позволяет определить точную трехмерную структуру органической молекулы. Путем измерения рассеяния рентгеновских лучей на атомах можно определить расстояния и углы между атомами и, таким образом, определить тип гибридизации.
3. Различные химические реакции:
Некоторые химические реакции могут помочь определить тип гибридизации в органических соединениях. Например, гидрогенирование может указать на наличие спиральной гибридизации, а гидролиз эфира - на этерную гибридизацию.
4. Квантово-химические расчеты:
С помощью квантово-химических методов, таких как DFT или МШФ, можно предсказать тип гибридизации атомов в органических соединениях. Эти методы основаны на расчете энергии и формы молекулы, что позволяет предсказать тип гибридизации.
Эти методы используются вместе для определения типа гибридизации в органических соединениях. Каждый метод имеет свои преимущества и ограничения, выбор зависит от типа соединения и доступности оборудования.
Сравнение гибридизации в органических соединениях

Существует несколько типов гибридизации, определяемых количеством и типом гибридных орбиталей для образования связей в молекуле. Основные типы: sp, sp2 и sp3.
Гибридизация sp характерна для молекул с двумя σ-связями и без свободных электронных пар. Примеры: ацетилен (C2H2), бериллийхлорид (BeCl2) и боран (BH3). Гибридизация sp обеспечивает линейную геометрию молекул.
Гибридизация sp2 характерна для молекул с тремя σ-связями и одной π-связью или без свободных электронных пар. Примеры: C2H4, CH2O, BF3. Эти соединения имеют плоскую треугольную геометрию.
Гибридизация sp3 характерна для молекул с четырьмя σ-связями или тремя σ-связями и одним свободным электронным паром. Примеры: CH4, C2H5OH, H2NCH2CH2NH2. Молекулы с гибридизацией sp3 имеют тетраэдрическую геометрию.
Анализ гибридизации позволяет определить тип связей, геометрию молекулы и химические свойства соединений. Понимание гибридизации помогает предсказывать реакционную способность молекул и их возможные реакции.
Некоторые случаи гибридизации могут отличаться от стандартных типов из-за особых электронных структур или молекулярной конфигурации.
Примеры гибридизации sp, sp2, sp3

Гибридизация sp: s- и p-орбитали сливаются в две гибридные орбитали. Примеры: CO2, C2H4.
Гибридизация sp2: s- и две p-орбитали сливаются в трех гибридные орбитали. Пример: C6H6.
Гибридизация sp3 характеризуется слиянием одной s-орбитали и трех p-орбиталей в четыре гибридные орбитали. Этот тип гибридизации встречается, например, в молекуле метана (CH4), где углерод атом образует четыре одиночные связи.
Знание типа гибридизации позволяет понять структуру и свойства органических соединений, а также предсказать их реактивность и возможные реакции.
Роль гибридизации в свойствах органических соединений
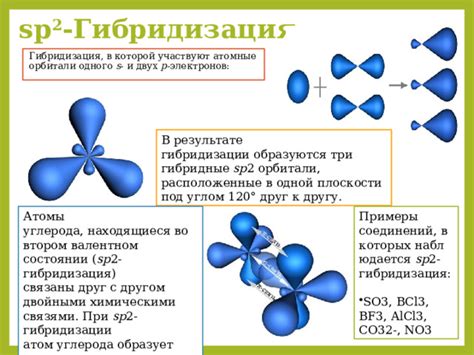
Одна из основных характеристик гибридизации - это число s- и p- орбиталей, участвующих в образовании гибридных орбиталей. В органической химии наиболее распространены гибридизации sp3, sp2 и sp.
Гибридизация sp3 характерна для атомов углерода, связанных с четырьмя различными атомами или группами. Образуются четыре гибридные орбитали в форме тетраэдра - это особенно часто встречается в алканах.
Гибридизация sp2 наблюдается у атомов углерода, связанных с тремя различными атомами или группами. Три гибридных орбитали образуют плоский треугольник. Четвертая p-орбиталь не участвует в образовании связей и может формировать пи-связи. Примеры органических соединений с гибридизацией sp2 - алкены и ароматические соединения.
Гибридизация sp встречается у атомов углерода, связанных с двумя различными атомами или группами. Две гибридные орбитали располагаются по двум противоположным сторонам атома углерода, образуя линейную геометрию. Представителями этой гибридизации являются алкины.
| Гибридизация | Число гибридных орбиталей | Примеры соединений |
|---|---|---|
| sp3 | 4 | алканы |
| sp2 | 3 | алкены, ароматические соединения |
| sp | 2 | алкины |
Гибридизация играет важную роль в определении свойств органических соединений, таких как их геометрия, химическая активность и способность образовывать связи.