Химия – это изучение состава, свойств и структуры вещества. Важное понятие в химии – масса вещества. Нередко нужно найти массу конкретного вещества, включая воду.
Вода – важное вещество для жизни на Земле, участвует во многих химических реакциях. Изучение ее массы в химии помогает понять ее роль в процессах.
Для определения массы воды в химии 8 класса нужно знать формулу воды (H2O) и молярную массу вещества, которая равна 18 г/моль.
Как найти массу воды в химии для 8 класса
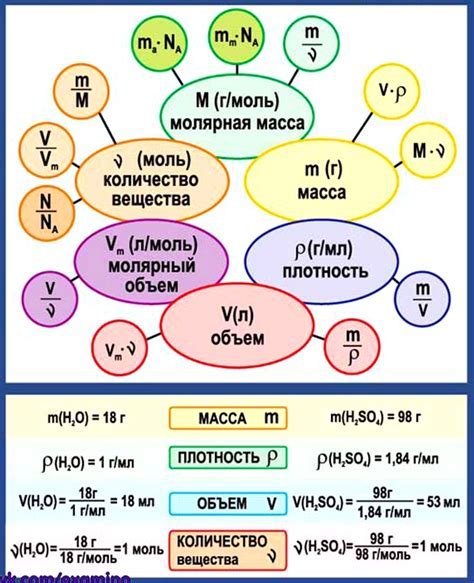
Определение массы воды в химии важно для решения задач, таких как расчет количества реагентов или продуктов реакции. Для этого используются различные методы и формулы.
Один из простых способов - использование формулы массовой доли. Массовая доля воды (W) вычисляется как отношение массы воды к общей массе раствора. Формула: W = (масса воды / общая масса) * 100%
Пример: есть раствор с 10 г воды и общей массой 50 г. Для расчета массовой доли воды применяем формулу: W = (10 г / 50 г) * 100% = 20%
Таким образом, массовая доля воды в этом растворе составляет 20%.
Масса воды может быть определена с использованием стехиометрических соотношений. Стехиометрия - это наука о количественных соотношениях в химической реакции. В соответствии с этим, массу воды можно вычислить на основе массы других веществ, участвующих в реакции.
Например, при анализе гидратов (веществ, содержащих молекулы воды), можно использовать их формулы для определения массы воды. Формула гидрата обычно записывается с точкой между молекулами гидрата и молекулами воды. Например, CuSO4 • 5H2O означает, что каждая молекула CuSO4 содержит 5 молекул воды.
Масса воды в гидрате может быть определена с использованием его молярной массы и формулы. Например, для CuSO4 • 5H2O молярная масса равна 249,68 г/моль. Для нахождения массы воды умножьте количество молекул воды (5) на молярную массу воды (18,02 г/моль):
- Масса воды = 5 * 18,02 г/моль = 90,1 г
Таким образом, масса воды в гидрате CuSO4 • 5H2O составляет 90,1 г.
Эти методы помогают определить массу воды в химии в 8 классе и использовать результаты для решения различных задач в химических расчетах.
Способы измерения массы воды
Второй способ - выпаривание. Вода нагревается до полного испарения, затем выпарившуюся воду можно собрать и измерить ее массу, например, с помощью весов.
Третий способ - использование пробирок и градуированных цилиндров. Вода помещается в пробирку или цилиндр и измеряется массой или объемом, который затем можно преобразовать в массу.
Независимо от выбранного способа измерения, необходимо учитывать погрешности и правильно проводить эксперимент, чтобы получить достоверные результаты.
Формула для расчета массы воды
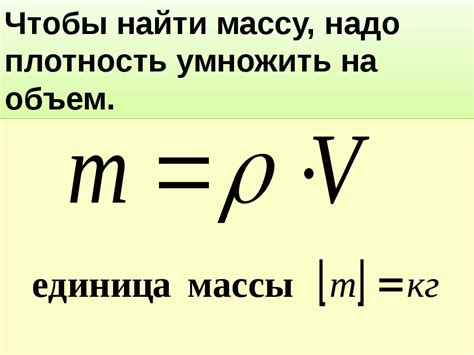
Масса воды может быть рассчитана с использованием формулы:
масса воды = объем воды × плотность воды
Объем воды указывается в литрах, а плотность воды равна 1 г/мл. Для удобства можно запомнить, что 1 литр воды массой равен 1000 г.
Расчет массы воды осуществляется следующим образом:
масса воды = объем воды (л) × плотность воды (г/мл)
Например, если необходимо рассчитать массу воды, имеющей объем 5 литров, то:
Масса воды = 5 л × 1 г/мл = 5000 г
Таким образом, масса воды составит 5000 г.
Примеры задач по расчету массы воды

Расчет массы воды может быть необходим при решении различных химических задач. Рассмотрим несколько примеров задач:
Задача 1:
Сколько массы воды содержится в 100 г раствора с солями, если содержание воды составляет 80% по массе?
Решение:
Масса воды в растворе равна 80% от массы раствора. Таким образом, масса воды будет равна:
Масса воды = 100 г * 80% = 80 г
Ответ: В растворе содержится 80 г воды.
Задача 2:
Какую массу воды можно получить в результате реакции сжигания 10 г метана (CH4)?
Решение:
При сжигании метана образуется два моля воды на один моль метана. Масса метана - 16 г/моль, масса воды - 18 г/моль.
Масса воды из 10 г метана:
1 моль CH4 = 2 моль H2O
16 г CH4 = Х г H2O
16 г * 1 моль/16 г = Х г * 2 моль/18 г
Х г = 16 г * 18 г/2 = 144 г
Ответ: При сжигании 10 г метана образуется 144 г воды.
Новая задача:
Сколько воды можно получить из реакции 20 г кальция и избытка воды?
Решение:
При реакции кальция с водой образуется 1 моль воды (H2O) на 1 моль кальция (Ca). Мольная масса кальция равна 40 г/моль.
Массу воды, получаемую из 20 г кальция, можно рассчитать следующим образом:
Мольная масса кальция = 40 г/моль
Мольные соотношения:
1 моль Ca = 1 моль H2O
40 г Ca = Х г H2O
Подставляем значения и находим Х:
40 г * 1 моль/40 г = Х г * 1 моль/18 г
40 г = 1/18 * Х г
Х г = 40 г * 18 г
Х г = 720 г
Ответ: Реакция 20 г кальция с избытком воды даст 720 г воды.