Существует много разных классов соединений в химии, одним из которых является кислоты, основания, соли и оксиды. Понимание, к какому классу относится вещество, помогает изучить его свойства и реакции.
Кислоты - это вещества, которые отдают протоны и образуют соли с основаниями. Основания принимают протоны от кислот и образуют соли. Соли образуются из реакции кислоты с основанием, протоны передаются основанию. Соли не обладают кислотными или щелочными свойствами.
Оксиды - соединения из двух элементов, один из которых - кислород. Они могут быть кислотными или основными, в зависимости от другого элемента. Кислотные оксиды образуют кислоты при реакции с водой, а основные оксиды могут образовывать основания при контакте с водой.
Определение класса вещества основывается на его химических свойствах и реакциях, а не только на названии. Для определения нужно изучить его формулу и молекулярную структуру, а также проанализировать взаимодействие с другими соединениями.
Знание о классификации соединений на кислоты, основания, соли и оксиды помогает понять их свойства и применение в химических процессах. Это основа для дальнейших исследований в химии.
Кислота
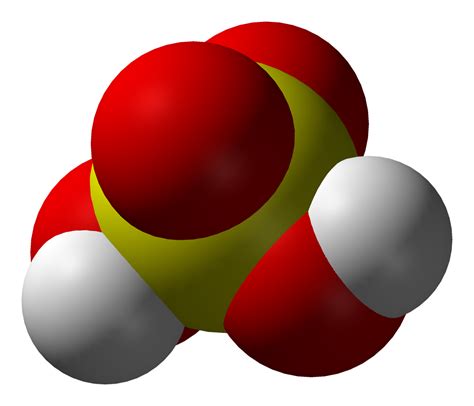
Кислоты бывают органическими или неорганическими. Органические кислоты содержат углерод и относятся к классу органических соединений. Примерами органических кислот являются уксусная, лимонная и салициловая кислоты.
Неорганические кислоты не содержат углерод и составляют большую часть всех кислот, таких как серная кислота, соляная кислота и солянокислый калий.
Кислоты бывают сильными или слабыми в зависимости от способности отдавать положительно заряженные ионы в растворе. Некоторые, как серная кислота, ионизируются полностью, а другие, такие как уксусная кислота, только отчасти.
Важно помнить:
- Кислоты обладают кислотными свойствами в растворах.
- Кислоты бывают органическими или неорганическими.
- Сильность кислоты зависит от её способности отдавать положительно заряженные ионы в растворе.
Изучение кислот и их свойств важно для химического образования и понимания реакций веществ.
Что такое кислота

Кислоты делятся на неорганические (минеральные) и органические. Минеральные кислоты получают из неорганических соединений, органические содержат углерод и получают, например, из растительных или животных продуктов.
Кислоты находят применение в химической промышленности, медицине, повседневной жизни, а также играют важную роль в химических реакциях и жизнедеятельности организмов.
Свойства кислот

1. Кислотность. Кислоты могут отдавать протоны в растворе.
2. Реакция с щелочами. Кислоты реагируют с щелочами, образуя соли и воду. Это называется нейтрализацией.
3. Реакция с металлами. Некоторые кислоты реагируют с металлами, выделяя водород.
4. Реакция с основаниями. Кислоты могут образовывать соли и воду с основаниями.
5. Когда кислоты диссоциируют в воде, они образуют H+ и анионы кислоты.
6. Многие кислоты разъедают материалы, такие как металлы и минералы, поэтому их нужно использовать осторожно.
Как определить кислоту

Для определения кислоты проводится химический анализ.
Сначала образец растворяется в воде. Затем добавляют индикатор кислотности, например, фенилфталеин. Фенилфталеин изменяет цвет: в кислом растворе он безцветный, в щелочном - розовый или фиолетовый.
Для определения концентрации кислоты нужно провести титрование. К конечному раствору с индикатором добавляют стандартный раствор щелочи или соли. При достижении точки эквивалентности происходит окрашивание раствора в розовый цвет.
| Реагенты | C | V |
|---|---|---|
| Образец кислоты | CA | VA |
| Индикатор кислотности | - | - |
| Стандартный раствор щелочи или соли | CB | VB |
где CА - концентрация исследуемой кислоты, VА - объем исследуемой кислоты, CВ - концентрация стандартного раствора щелочи или соли, VВ - объем стандартного раствора щелочи или соли.
Для расчета концентрации исследуемой кислоты используется формула:
CА * VА = CВ * VВ
После всех операций и расчетов можно определить концентрацию кислоты.
Основание

Основания могут быть естественного или искусственного происхождения. Естественные основания это гидроксиды (гидроксид натрия, гидроксид калия) и неорганические соли (некоторые соли аммония).
Искусственные основания, или щелочи, создаются химическими реакциями или обработкой минералов и широко применяются в различных областях.
Основания можно легко отличить от кислот и солей по нескольким признакам. Они имеют щелочной вкус и реакцию, могут окрашивать лакмус в зеленый цвет, образовывать медленно растворимые соли и быть определены при помощи pH метра.
Концентрация основания в растворе может сильно варьировать в зависимости от его состояния и условий растворения. Для определения основания необходимо провести химические и физические анализы.
Что такое основание
Основания отличаются от солей и оксидов тем, что они могут быть щелочными и растворяться в воде, образуя щелочные растворы. Щелочные растворы имеют высокий pH и могут нейтрализовать кислоты.
Основания также могут быть амфотерными и реагировать как с кислотами, так и с основаниями. Например, гидроксиды аммония или амфотерный окись алюминия могут образовывать соли и реагировать с кислотами.
| Примеры оснований | Химическая формула |
|---|
| Гидроксид натрия | NaOH |
| Гидроксид калия | KOH |
| Гидроксид аммония | NH4OH |
| Гидроксид кальция | Ca(OH)2 |
| Гидроксид магния | Mg(OH)2 |
Основания играют важную роль в химии и используются в различных областях, например в производстве мыла и моющих средств, в аналитической исследовательской химии, а также в медицине и фармацевтике.
Свойства оснований

- Основания обладают щелочной реакцией. Они способны нейтрализовать кислоты, образуя соль и воду. Реакция основания с кислотой называется кислотно-щелочной реакцией.
- Основания разлагаются при нагревании. При нагревании основания распадаются на оксиды и воду.
- Основания имеют горький вкус и могут образовывать мыльные растворы. Благодаря присутствию оснований в мыле, оно может очищать от грязи.
- Основания изменяют цвет индикаторов. Некоторые индикаторы меняют цвет при контакте с основанием, например, фенолфталеин становится красным в щелочной среде.
- Основания легко растворяются в воде. Они образуют щелочные растворы из-за их высокой растворимости в воде.
Зная эти свойства оснований, можно определить их в растворе и изучить взаимодействие с другими веществами.
Как определить основание
- Используйте индикатор кислотности: Положите немного вещества, которое вы считаете основанием, на фильтровальную бумагу или полоску индикатора, затем погрузите вещество в раствор кислоты. Если вещество окрасится в другой цвет, это может свидетельствовать о наличии основания.
- Проведите нейтрализационную реакцию: Смешайте небольшое количество кислоты с веществом, которое вы предполагаете основанием. Если произошло выделение тепла, пузырьков газа или образование осадка, это может указывать на наличие основания.
- Изучите свойства вещества: Основания имеют определенные свойства, которые могут помочь в их определении. Например, основания способны нейтрализовать кислоту и обладают щелочной реакцией, изменяя значение pH раствора. Также они часто образуют гидроксиды или оксиды металлов.
Если вы неуверены, является ли вещество основанием, рекомендуется провести дополнительные химические эксперименты или обратиться к врачу или учителю химии для получения дополнительной информации и помощи.