Буферный раствор удерживает постоянный уровень pH при добавлении кислот и щелочей благодаря наличию слабых кислот и их соединений, которые реагируют с добавленными веществами.
Принцип работы буферного раствора заключается в сопряженных кислотах и основаниях. Буферный раствор состоит из слабой кислоты и ее сопряженного основания. Когда добавляется кислота, они реагируют, чтобы поглотить избыточные ионы водорода (Н+), поддерживая постоянное pH. При добавлении щелочи они реагируют с гидроксидными ионами (ОН-), чтобы поддерживать стабильный pH.
Буферные растворы применяются в медицине, биологии и химических процессах. В медицине они обеспечивают стабильность pH в образцах крови и тканей. В исследованиях биологии они поддерживают постоянные условия окружающей среды для изучения реакций в клетках и организмах.
Что такое буферный раствор
Буферный раствор помогает минимизировать изменения pH при добавлении кислоты или щелочи. Он содержит слабую кислоту и конъюгированную слабую щелочь или наоборот. Эти компоненты поглощают добавленные ионы H+ или OH- и предотвращают значительное изменение pH.
Бикарбонатный буфер, фосфатный буфер и ацетатный буфер - самые известные примеры буферных растворов. Бикарбонатный буфер поддерживает постоянство pH в крови, фосфатный буфер используется в молекулярной биологии, а ацетатный буфер - в биохимических исследованиях.
Буферные растворы имеют предел стабильности и не могут поддерживать постоянное pH при слишком высоких или низких значениях кислотности и щелочности.
Принцип работы буферного раствора

При добавлении кислоты к буферному раствору происходит реакция с его слабой основой, образуя соль и воду. Таким образом, изменение pH раствора остается минимальным. При добавлении щелочи, реагирующей со слабой кислотой, также образуется соль и вода. Эта комбинация реакций помогает буферному раствору поддерживать постоянное pH.
Примером буферного раствора является система угольной кислоты и ее соли – бикарбонат. В организме человека гидрокарбонатная система играет важную роль в поддержании стабильного pH крови. Если кровь становится слишком кислой, бикарбонат-ионы нейтрализуют кислоты, превращая их в углекислоту, которая выводится через легкие. Аналогично, если кровь становится слишком щелочной, углекислота превращается обратно в бикарбонат-ионы, которые выделяются через почки.
Буферные растворы поддерживают оптимальный pH в организмах живых существ, обеспечивая нормальное функционирование химических процессов.
| Преимущества буферных растворов | Примеры буферных растворов |
|---|---|
| - Поддерживают постоянный pH | - Уксусная кислота и ее соль |
| - Снижают изменение pH | - Фосфатная кислота и ее соли |
| - Играют важную роль в биологических процессах | - Гидрокарбонатная система в крови |
Какие вещества могут быть использованы в буферном растворе

Буферный раствор - это раствор, содержащий вещества, способные реагировать с кислотами или щелочами для поддержания постоянного pH. В качестве буферных веществ могут использоваться соединения в форме кислот и их солей или щелочей и их солей.
Наиболее распространенные буферные вещества включают карбонатные буферы, фосфатные буферы, ацетатные буферы и трис-буферы.
- Карбонатные буферы: Карбонатные буферы используют карбонат и бикарбонат в качестве буферных веществ и работают в диапазоне pH от 9 до 10.
- Фосфатные буферы: Эти буферы содержат гидрофосфат и дигидрофосфат в качестве буферных веществ и широко применяются в биохимических и медицинских исследованиях для обработки кислотных и щелочных реакций.
- Ацетатные буферы: Используют ацетат и его соль для поддержания pH от 4,5 до 5,5.
- Трис-буферы: Используют трис и его соль для стабильного pH от 7 до 9.
Выбор буферного вещества зависит от pH раствора и его использования. Каждое вещество имеет оптимальный диапазон pH, при котором оно работает наилучшим образом. Необходимо учитывать также условия использования, такие как температура и другие реагенты.
Реакция буферного раствора с добавлением кислоты

При добавлении кислоты в буферный раствор происходит процесс нейтрализации. Кислота донорного компонента буферного раствора реагирует со щелочью акцепторного компонента, образуя соль и воду. Например, в случае буферного раствора ацетата натрия, кислотой будет уксусная, а щелочью - гидроксид натрия.
Донорный компонент буферного раствора связывается с ионами водорода H+, образуя неионизированную форму кислоты. Это уменьшает концентрацию H+ и поддерживает постоянный уровень pH в растворе. Акцепторный компонент раствора служит резервуаром для H+ и помогает нормализовать pH.
Примером реакции буферного раствора с добавлением кислоты может быть рассмотрение системы уксусной кислоты и ацетата натрия. При добавлении малого количества кислоты, уксусная кислота реагирует с ацетатом натрия, образуя нейтральный уксусный остаток и донорный компонент ацетатного иона:
CH3COOH + H3O+ → H2O + CH3COO-
В результате этой реакции концентрация H+ снижается и pH раствора остается постоянным, благодаря взаимодействию между донорным и акцепторным компонентами буфера.
Реакция буферного раствора с добавлением щелочи

Буферный раствор играет важную роль в регулировании pH среды. Когда в буферный раствор добавляется щелочь, происходит особая реакция, которая позволяет поддерживать стабильное pH.
Буферный раствор состоит из слабой кислоты и соответствующей соли или слабого основания и его соответствующей соли. Когда щелочь добавляется в буферный раствор, щелочь реагирует со слабой кислотой или ее солью, образуя основание и воду.
Реакция выглядит следующим образом:
База + Кислота ↔ Основание + Вода
Например, если в буферный раствор добавляется щелочь, щелочь реагирует со слабой кислотой в растворе, образуя основание и воду:
NaOH + CH3COOH ↔ CH3COONa + H2O
В этом примере щелочь NaOH реагирует с уксусной кислотой CH3COOH, образуя уксусную соль CH3COONa и воду H2O. Эта реакция позволяет раствору поддерживать стабильный pH.
Буферный раствор с добавлением щелочи важен для многих биологических процессов, таких как поддержание pH в крови и переваривание в желудке.
Использование таких растворов помогает контролировать и поддерживать оптимальный pH в различных системах.
Значение pH в буферном растворе
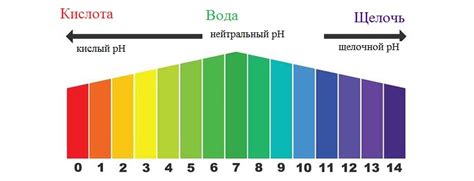
- Раствор с pH менее 7 - кислотный;
- Раствор с pH 7 - нейтральный;
- Раствор с pH более 7 - щелочной.
Буферный раствор сохраняет своё pH значение при добавлении кислоты или щелочи благодаря присутствию слабой кислоты и её соли или слабой щелочи и её соли. Они играют важную роль в биологических процессах, так как системы требуют устойчивого pH для нормального функционирования.
Примером буферного раствора является бикарбонатный буфер, содержащий бикарбонат (HCO3-) и конъюгированную кислоту (CO2). Он широко распространен в организме живых существ и помогает поддерживать уровень pH в норме.
Примеры использования буферного раствора

Буферные растворы широко применяются в различных областях науки и техники. Они представляют собой растворы, способные поддерживать постоянный pH, даже при добавлении кислоты или щелочи. Вот несколько примеров использования буферного раствора:
1. Биология и биохимия: Буферные растворы используются для поддержания стабильного pH в экспериментах с биологическими системами, например, при культивировании клеток или изучении ферментативных реакций. Они также применяются в молекулярной биологии, чтобы обеспечить оптимальные условия для проведения реакций ПЦР или электрофореза ДНК.
2. Химический анализ: Буферные растворы используются для калибровки pH-метров и поддержания стабильных условий при проведении реакций, например, в газохроматографии.
3. Фармацевтика: Буферные растворы применяются в производстве лекарств для регулирования pH и обеспечения стабильности препаратов, а также в исследованиях фармакокинетики и фармакодинамики.
4. Аналитическая химия: Буферные растворы применяются в аналитической химии для установления стабильных условий и предотвращения изменения pH в ходе анализа образцов. Они используются, например, при определении концентрации ионов в растворе с помощью потенциометрических измерений или при проведении титриметрии.
Примеры использования буферного раствора показывают его важность в различных областях науки и техники, где требуется поддерживать стабильное pH для достижения точных результатов и предотвращения нежелательных изменений.