Химия – это наука, которая изучает состав вещества и его превращения. Всем известно, что любое вещество состоит из атомов. Масса атома является одним из ключевых параметров, которые помогают понять и описать свойства вещества. Найти массу атома может показаться сложной задачей, но на самом деле это довольно просто, если вы знаете несколько основных принципов.
Первое, что вам нужно знать, это атомная масса. Атомная масса – это средняя масса атома элемента, выраженная в атомных единицах. Для поиска атомной массы вам необходимы таблицы Менделеева, где указаны атомные массы всех элементов. Найдите интересующий вас элемент в таблице и узнайте его атомную массу.
Далее, вы должны знать количество атомов в молекуле. В молекуле обычно содержится несколько атомов одного или разных элементов. Чтобы найти массу атома в молекуле, необходимо умножить атомную массу элемента на количество атомов данного элемента в молекуле. Таким образом, вы сможете определить общую массу атомов в молекуле.
Итак, чтобы найти массу атома в химии, необходимо знать атомную массу элемента и количество атомов данного элемента в молекуле. Эти простые принципы помогут вам легко и точно расчитать массу атома и понять его значение при изучении и описании вещества.
Что такое масса атома?

Массу атома можно рассчитать, зная его атомный номер и молярную массу элемента. Атомный номер - это количество протонов в ядре атома, а молярная масса - это средняя масса атомов элемента в единице измерения, которая равна грамму на моль (г/моль).
Для атома кислорода атомный номер - 8, а молярная масса - примерно 16 г/моль. Масса атома кислорода - примерно 2,67 а.е.
Масса атома играет важную роль в химических реакциях и расчетах, так как помогает определять количество вещества, молярную массу и другие характеристики элемента или соединения.
Определение и значение

Подсчет массы атома
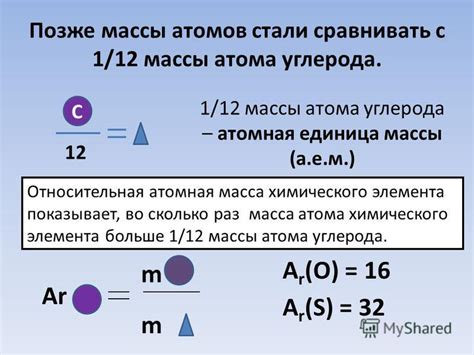
- Найти протонное число атома, равное количеству протонов в ядре атома.
- Определить нейтронное число атома, равное количеству нейтронов в ядре атома.
- Рассчитать массовое число атома, сложив число протонов и число нейтронов.
- Перевести массовое число в граммы, зная, что 1 а.е.м. равно примерно 1,67 x 10-24 г.
Таким образом, зная порядковый номер элемента и количество нейтронов, можно рассчитать массу атома данного элемента. Зная массу атома, можно провести дальнейшие расчеты и анализы в области химии и физики.
Формула и методы расчета массы атома

Масса атома в химии измеряется в атомных массах или Дальтонах (Да). Для расчета массы атома используется формула:
Масса атома (Ма) = Молярная масса (Мм) / Авогадро число (Na)
Молярная масса - это масса одного моля вещества, которая измеряется в граммах на моль (г/моль). Авогадро число (Na) равно 6,022 × 10^23 частиц в одном моле вещества.
Существуют различные методы для определения молярной массы вещества:
- Аналитический метод: Определяется путем экспериментов с использованием химического анализа и специальных инструментов, таких как масс-спектрометры.
- Теоретический метод: Расчет молярной массы основывается на атомарной массе каждого элемента, умноженной на его количество в молекуле вещества. Затем все массы суммируются для получения общей массы.
Некоторые химические элементы имеют переменную массу атома из-за наличия изотопов. Для таких элементов необходимо учитывать относительное количество каждого изотопа при расчете молярной массы. Это делается путем умножения массы каждого изотопа на его относительную абундантность, выраженную в процентах.
Зная массу атома, химики могут проводить различные вычисления и определять пропорции веществ в химических реакциях, что позволяет им понять, какие процессы происходят на молекулярном уровне.
Значение массы атома в химических расчетах
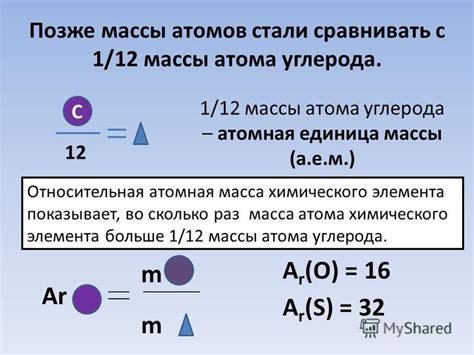
Знание массы атома является ключевым для различных химических расчетов. Например, масса атома используется для определения молярной массы вещества, которая определяет количество вещества в молях. Также, масса атома влияет на результаты реакций, так как при расчетах учитывается соотношение массы вещества и количество вещества.
Массу атома можно найти в периодической системе химических элементов. Разница между массой атомов разных элементов обусловлена количеством протонов и нейтронов. Изменение массы атома может быть вызвано изотопами элемента, которые имеют различную массу.
Для точных химических расчетов нужно использовать точные значения масс атомов. В периодической системе химических элементов указаны средние значения масс атомов с учетом изотопического состава. Однако для более точных расчетов можно использовать экспериментальные данные для конкретного изотопа.