Окисление металлов - это процесс, во время которого они вступают в реакцию с кислородом, образуя соединения, называемые оксидами. Каждый металл имеет определенную высшую и низшую степень окисления, которые могут быть полезными при изучении и предсказании его химического поведения.
Узнать высшую степень окисления металла можно, обратив внимание на его расположение в периодической таблице. Обычно металлы справа и наверху таблицы имеют более высокую степень окисления, поскольку они имеют больше электронных оболочек и могут потерять или передать больше электронов. Таким образом, металлы, расположенные в верхней правой части периодической таблицы, имеют высшую степень окисления.
Другим способом определения степени окисления металла является анализ его соединений. Нужно обратить внимание на ион металла в соединении и окружающие его атомы. Например, если металл образует ион с зарядом +3 и окружен тремя атомами кислорода, то его степень окисления равна +3.
Окисление металлов: суть процесса

Окисление металлов происходит в различных условиях и зависит от температуры, концентрации окислителя, присутствия каталитических веществ и других факторов. Скорость процесса может быть разной в зависимости от условий.
Окисление металлов играет важную роль в нашей жизни, так как мы часто используем их в различных отраслях, таких как строительство, промышленность и электроника. Например, алюминий образует защитную пленку оксида на своей поверхности, что делает его стабильным и устойчивым к коррозии.
Однако окисление металлов также может быть нежелательным. Коррозия металлов, вызванная их окислением, часто приводит к повреждению и разрушению металлических конструкций. Например, железо окисляется воздухом и влагой, образуя ржавчину.
Высшая степень окисления: определение
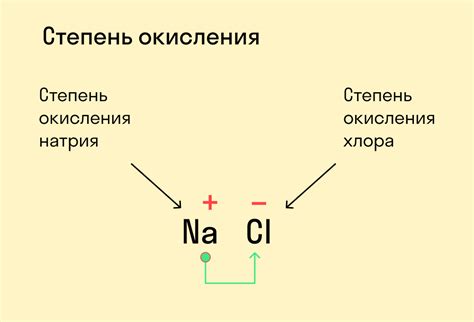
Определение высшей степени окисления важно для понимания химических свойств элементов и их соединений. Оно позволяет определить тип взаимодействия металла с другими элементами, а также предсказать возможные реакции, включающие данный металл.
Высшая степень окисления может быть определена на основе полиатомных и металлических соединений. При анализе соединений металла с различными неокисными элементами, такими как водород, кислород, азот и сера, можно установить наибольшее количество электронов, которые металл способен потерять.
Определение высшей степени окисления может быть связано с активностью металлов. Ряд активности упорядочивает металлы по способности образовать положительные ионы. Металлы с меньшей активностью имеют низшие степени окисления, а с большей активностью – более высокие.
Метод массивного определения высшей степени окисления

Этот метод используется для определения максимальной степени окисления металлов в соединениях. Он основан на реакциях металлических катионов с ионами галогенов.
Для проведения массивного метода необходимы соединения металлов с разными степенями окисления и растворы галогенов. Металлический катион вступает в реакцию с ионами галогена и образует соединение с наибольшей степенью окисления. При этом другие металлические катионы остаются без изменений или образуют соединения с меньшей степенью окисления.
После проведения реакции анализируют образовавшиеся соединения. Металл с наибольшей степенью окисления будет присутствовать только в одном из них. Остальные соединения будут содержать металлы с меньшей степенью окисления.
Массивный метод определения высшей степени окисления позволяет получить точный результат и может быть использован для определения высшей степени окисления металлов в различных соединениях.
Метод с использованием ионной формулы

Ионная формула - запись соединения в виде ионов. Например, для хлорида калия - K+Cl-. Знак "+" у иона калия указывает на положительный заряд, "-" у иона хлорида - на отрицательный.
Чтобы определить высшую степень окисления металла, нужно знать его положительный заряд в данном ионе. Например, в хлориде калия ион калия имеет заряд "+", значит, калий имеет степень окисления +1.
Металлы могут иметь разные степени окисления в разных соединениях. Например, у меди могут быть степени окисления +1 и +2. Тут важно знать правила и использовать таблицы соответствия степеней окисления.
Используя ионную формулу, можно точно определить высшую степень окисления металлов и использовать эту информацию в химических расчетах и реакциях.
Определение высшего окисления по структурной формуле

Высшая степень окисления металла в соединении можно определить по его структурной формуле:
Шаг 1: Изучите структурную формулу соединения металла, учитывая его положительный заряд.
Шаг 2: Определите атом металла с наибольшим количеством кислородных атомов, обычно это атом с наименьшей суммой коэффициентов.
Шаг 3: Определите степень окисления металла, используя найденные данные.
Рассчитайте высшую степень окисления металла, учитывая заряды металла и кислорода. Учитывайте заряды других атомов при расчете.
Шаг 4:
Запишите высшую степень окисления металла в соединении в виде арабской цифры или римской цифры в верхнем индексе у символа металла.
Например, для соединения Fe2O3 (оксид железа(III)):
Железо (Fe) имеет наименьшую сумму коэффициентов при кислороде, а именно 3. Следовательно, высшая степень окисления железа равна III.
Примеры определения высшего окисления металлов

Пример 1:
Высшее окисление металлов можно проиллюстрировать на примере окисления хрома (Cr). Хром формирует соединение, в котором его окисление достигает +6. Это соединение называется хромат(VI) калия и имеет формулу K2CrO4.
Пример 2:
Для определения окисления марганца (Mn) можно рассмотреть оксиды с разными степенями окисления. Самой высокой степенью окисления для марганца является +7. Оксид марганца(VII) имеет формулу Mn2O7.
Пример 3:
Высшая степень окисления металлов может быть определена на примере их соединений. Например, железо (Fe) может образовывать различные оксиды, но наибольшую степень окисления +3 имеет соединение феррит(III) (FeCl3), где окисление указывается в римской цифре перед названием.
Знание высшей степени окисления металла полезно в химической и аналитической химии, так как позволяет определить его реакционные свойства и взаимодействие с другими веществами.
Применение информации о высшей степени окисления

Одним из основных применений данной информации является прогнозирование межмолекулярных реакций. Зная высшую степень окисления металла, можно предсказать, какие реакции он будет совершать, например, окислительные или образование комплексных соединений.
Высшая степень окисления металла также позволяет определить его окислительно-восстановительные свойства. Металлы с более высокой степенью окисления обычно обладают большей способностью образовывать ионы. Это знание может быть полезным при выборе металла для проведения определенной реакции или при исследовании свойств различных металлических соединений.
Информация о высшей степени окисления может помочь предсказать растворимость металлических соединений. Металлы с более высокой степенью окисления чаще образуют растворимые соединения, чем металлы с более низкой степенью окисления. Это знание полезно при разработке новых материалов и исследовании свойств существующих соединений.
Информация о высшей степени окисления металлов помогает понять и предсказать химические свойства и реакции металлических соединений. Её можно использовать в различных областях, включая синтез новых соединений, анализ и исследование материалов.